てんかんの検査と治療
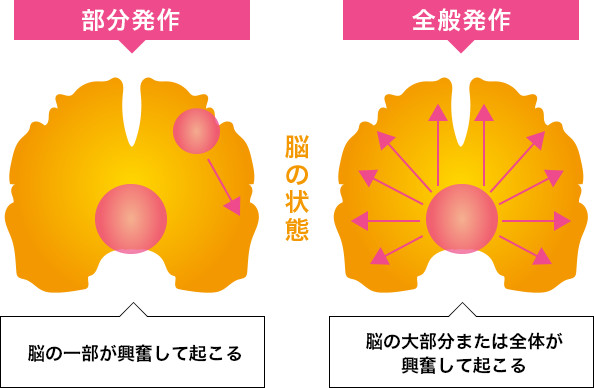
てんかんの最も重要な検査は、脳波検査で、てんかんによる特徴的な電気信号をとらえます。また、脳に何らかの問題がないかを確認するためにMRI検査やCT検査をしたり、原因を探索するために血液や尿検査をする場合もあります。
てんかんの主な治療は、薬物治療です。適切な服薬を行うことで、7~8割の患者さんは症状をコントロールできます。一方で、約2割の患者さんでは、薬物治療がききにくい「難治性てんかん」といわれています。
当院では、脳神経内科のほか、小児神経科医師(非常勤)による診察も行っています。